- ÚVOD
- NAŠA MISIA
- PARTNERI
- NOVINKY
- PREVENCIA A LIEČBA
- Rakovina hrubého čreva a konečníka
- Rakovina pankreasu
- Kolonializmus a rakovina
- Nanomedicína
- Výzvy v liečbe karcinómu pankreasu
- Najčastejšie príznaky nádorov gastrointestinál-
neho traktu - HISTÓRIA
- VÝSLEDKY
- FOTOGALÉRIA
- SPOLUPRÁCA
- VIZUÁLNA IDENTITA
- KONTAKT
NANOMEDICÍNA
Nanomedicína je relatívne nové, dynamicky sa rozvíjajúce odvetvie medicíny, ktorého cieľom je zlepšiť diagnostiku a liečbu multifaktoriálne podmienených ochorení. Je to interdisciplinárna veda, ktorá spája znalosti biomedicínskych vied (molekulárna biológia, genetika, farmácia, medicína) s poznatkami z nanotechnológie a vedy o materiáloch.
Nanomateriály
Nanomateriál je materiál, ktorého najmenej jeden rozmer má veľkosť v rozpätí 1 až 100 nm. V prípade nanomedicíny sa táto všeobecne akceptovaná definícia rozširuje aj na častice s rozmermi do 1 000 nm. Dôvodom sú povrchové úpravy, ktoré sú nevyhnutné pre ich aplikáciu v medicíne. Nanomatierály sa vyznačujú unikátnymi fyzikálno-chemickými vlastnosťami (elektrické, tepelné, magnetické, vodivé, optické a iné), ktoré materiál, z ktorého sú vyrobené, nemá. Ich charakteristickou črtou je veľký povrch v pomere k objemu. Táto skutočnosť spôsobuje, že povrch nanomateriálov je veľmi reaktívny, čo spôsobuje, že sa jednotlivé častice rýchlo zhlukujú do väčších útvarov, agregátov. Tento fenomén je prekážkou pre biomedicínske aplikácie, preto sa povrch nanomateriálov upravuje rôznymi zlúčeninami, ktoré znižujú zhlukovanie a zároveň zvyšujú ich biokompatibilitu (znášanlivosť v biologickom prostredí). Fyzikálno-chemické vlastnosti (veľkosť, tvar, povrchová úprava, náboj a iné) sú kľúčovými parametrami, ktoré ovplyvňujú spôsob vstupu nanomateriálu do bunky, jeho biodistribúciu a odbúravanie z organizmu.
Nanomateriály využívané v medicíne môžu mať organický alebo anorganický pôvod. Medzi najčastejšie skúmané a používané organické nanonosiče patria lipozómy, polymérne nanočastice, micely, dendriméry, alebo nanogély (Obr. 1).
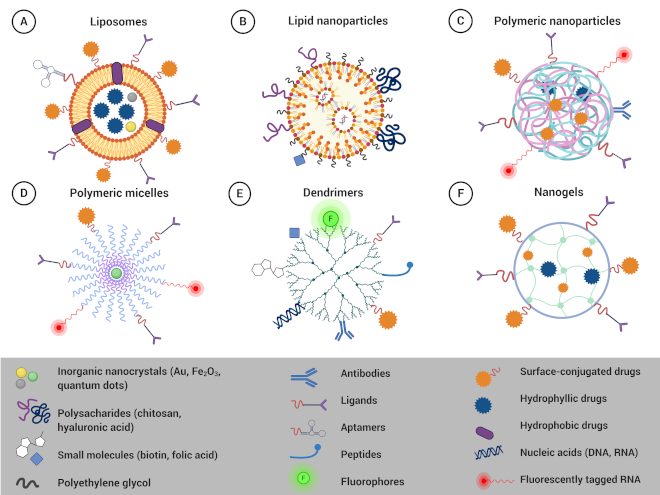
Obr. 1. Organické nanonosiče (Zdroj: Boucikova et al., Cancers (Basel) 2020 Dec 3;12(12):3622. doi: 10.3390/cancers12123622)
Organické nanonosiče ako prvé dostali povolenie od regulačných úradov (US FDA – Food and Drug Administration, EMA – European Medical Agency) na použitie v klinickej praxi. V súčasnosti sa v onkológii využíva viac ako 50 liečiv na báze nanomateriálov (nanoliečivá) a viac ako 77 nových nanoproduktov sa testuje v rôznych klinických štúdiách (fáza I – III). K nanoliečivám, používaným v onkológii, patria napr. Doxil®/Caelyx™, Myocet®, DaunoXome®, Marqibo®, Mepact® alebo Onivyde® (nanoliečivá na báze lipozómov), Adagen®, Cimzia®, Macugen®, Neulasta®, Pegasys®, PegIntron®, Renagel®, alebo Somavert® (nanoliečivá na báze polymérov), Copaxone®, Eligard®, Estrasorb™, Oncaspar®, Krystexxa®, Plegridy®, Adynovate® (nanoliečivá na báze miciel) a Abraxane® (albumín naviazaný na paclitaxel).
Z anorganických nanomateriálov sa najviac skúmajú nanočastice na báze vzácnych kovov ako je zlato, striebro alebo platina. Oxidy kovov (oxidy železa: magnetit, maghemit) boli schválené ako kontrastné činidlá pre magnetickú rezonanciu (MRI) (e.g. Endorem, Sinerem, Resovist), alebo na liečbu anémie (napr. Feraheme).
Veľkosť nanomateriálov (~10-9 m) je porovnateľná s rozmermi biologicky dôležitých molekúl ako sú proteíny, molekuly DNA, RNA, lipidy, čím môžu relatívne ľahko preniknúť do buniek. Práve tieto ich jedinečné vlastnosti otvárajú nové možnosti presnejšej diagnostiky ochorenia a zlepšenia jeho liečby. Intenzívny biomedicínsky výskum sa venuje využitiu nanomateriálov ako kontrastných látok v zobrazovacích technikách (magnetická rezonancia, počítačová tomografia a iné), vo včasnej neinvazívnej diagnostike prostredníctvom biosenzorov, alebo ako efektívnych nosičov rôznych druhov liečiv. Nanonosiče umožňujú cielený transport liečiva do miesta určenia (nádor, poškodené tkanivo), čím dokážu účinne znížiť nepriaznivé vedľajšie účinky terapie. Včlenenie lipofilných (zle rozpustných vo vode) liečiv do nanonosičov navyše zlepšuje ich distribúciu, a chráni liečivá pred predčasným metabolizmom mimo cieľového miesta. Nanomateriály sú atraktívnym nástrojom na prekonanie prirodzených biologických bariér, ktoré sú často prekážkou pre efektívny transport liečiva do orgánu (napr. prestup liečiva do mozgu). Nová generácia nanoliečiv, označovaných ako teranostiká (theranostics = therapy + diagnostics), spája diagnostiku a liečbu do jednej platformy. Teranostikum obsahuje prvok, ktorý umožňuje lokalizovať nosič v cieľovom tkanive a následne tak sledovať liečebný proces (napr. zmenšovanie nádoru).
Bezpečnosť nanomateriálov
Nanomateriály používané v klinickej praxi musia spĺňať prísne bezpečnostné kritéria. Nesmú byť toxické, vyvolávať imunitnú odpoveď v organizme, musia byť biokompatibilné a stabilné. Ich schváleniu predchádza náročné testovanie v predklinických (modelové organizmy in vitro a in vivo) a klinických štúdiách (testovanie na pacientoch).
Pri posudzovaní biologickej bezpečnosti majú nanomateriály, v porovnaní s chemickými látkami, osobitné postavenie. Okrem chemického zloženia zohrávajú dôležitú úlohu pri odpovedi organizmu na expozíciu aj ich fyzikálne vlastnosti. Na komplexné preskúmanie potenciálneho biologického rizika sa používa séria testov odporúčaných Organizáciou pre hospodársku spoluprácu a rozvoj (OECD). Sú zamerané na potenciálnu cytotoxicitu, imunotoxicitu a genotoxicitu týchto látok. Testy in vitro sú v prevažnej miere realizované na bunkových líniách, pričom sú zvyčajne rýchle a relatívne ekonomicky nenáročné. V súčasnosti sa pristupuje k využívaniu pokročilejších mnohobunkových modelov, ktoré lepšie zohľadňujú komplexnosť organizmu a lepšie simulujú podmienky v organizme. Napriek tomu nemožno použitie in vivo, prevažne myších, modelov ešte úplne vylúčiť.
Využitie nanomateriálov v medicíne
Diagnostika
Pre efektívnu liečbu ochorenia je kľúčová včasná a presná diagnostika. Sľubným nástrojom v tejto oblasti sú práve nanomateriály. Vďaka nanotechnológii boli do klinickej praxe zavedené viaceré kontrastné činidlá, ktoré rozširujú neinvazívne spôsoby zobrazovacej diagnostiky (magnetická rezonancia MRI, pozitrónová emisná tomografia PET, ultrazvuk, fotoakustický prístup a pod.). Každá zo spomínaných zobrazovacích metód má svoje výhody, ale aj obmedzenia. Preto sa výskum zameriava na vývoj takých kontrastných látok, ktoré umožnia kombináciu viacerých zobrazovacích metód, čo prispieva k zlepšeniu a spresneniu lokalizácie patologických zmien.
Vďaka poznatkom z oblasti molekulárnej biológie boli identifikované viaceré kľúčové molekuly (biomarkery), ktoré sú úzko spojené s patogenézou niektorých ochorení. Takéto biomarkery v kombinácii s nanotechnológiou viedli k vývoju biosenzorov, ktoré sú schopné odhaliť viaceré ochorenia v skorých štádiách. Nanobiosenzory, využívajúce nanočastice zlata alebo kremíka, umožňujú včasnú diagnostiku niektorých neurodegeneratívnych ochorení ako napr. Alzheimerova, Parkinsonova alebo Creutzfeldt-Jacobsova choroba. Diagnostické čipy pre mnoho ďalších sú v štádiu vývoja.
Liečba
Regeneratívna medicína
Regeneratívna medicína je široká interdisciplinárna veda, ktorej cieľom je obnoviť poškodené alebo opotrebované bunky a tkanivá do stavu, ktorý čo najviac zodpovedá ich pôvodnej architektúre a funkcii. Nanomateriály nachádzajú veľké uplatnenie pri regenerácii kostí a chrupaviek. Chrupavka je tkanivo, ktoré nemá krvné a lymfatické cievy. Chondrocyt, základná bunková zložka chrupavky, je vyživovaný a zásobovaný kyslíkom len difúziou cez medzibunkovú hmotu, ktorá ho obklopuje. Rekonštrukcia poškodenej chrupavky je preto značne obmedzená a spočíva v transplatácii chondrocytov na povrch implantátu. Využitie nanomateriálov pri úprave povrchov kostných implantátov a chrupaviek umožňuje napodobniť prirodzené prostredie, čo uľahčuje mobilitu, prichytenie a diferenciáciu chondrocytov. Pri regenerácii chrupavky sa využívajú biomateriály, ako napr. kolagén, fibrín, alebo alginát. Prichyteniu buniek k matriciam implantátov napomáha povrchová topografia, nanolitografia. Výhodou niektorých nanomateriálov je ich antibakteriálna funkcia. Bežným problémom protéz sú totiž baktérie, ktoré sa nachádzajú na povrchu implantátov. Nanoštrukturované titánové povrchy napríklad zabraňujú kolonizácii takýchto patogénov.
Zubné lekársko je ďalším odvetvím medicíny, kde nanomateriály nachádzajú čoraz častejšie využitie. Nanodentológia je rýchlo sa rozvíjajúca oblasť medicíny, ktorá prináša novú generáciu technologicky vyspelých klinických nástrojov a zariadení pre orálnu zdravotnú starostlivosť. Nanomateriály nachádzajú uplatnenie pri remineralizácii zubnej skloviny pri oprave kazov alebo ako dentálne implantáty. V súčasnosti sú už komerčne dostupné produkty na báze nanomateriálov (Ostim®, VITOSSO™ alebo NanOSS™), ktoré sa používajú v regeneračnej stomatológii.
Enkapsulácia buniek
Pojem „bunková enkapsulácia“ znamená imobilizáciu buniek v polymérnych mikroguľôčkach alebo mikrokapsuliach, ktorá umožňuje ich transplantáciu do ľudských a zvieracích subjektov. Výhodou enkapsulácie je, že pacient nemusí užívať lieky, ktoré potláčajú imunitnú odpoveď (imunosupresíva), aby nedošlo k odvrhnutiu transplantátu. Kapsula umožňuje bunkám prijímať živiny a kyslík difúziou a eliminovať splodiny metabolizmu, pričom ochraňuje bunky pred deštrukciou imunitným systémom. Prvé implantovateľné mikrokapsule boli pripravené na liečbu cukrovky. Klinické testy (fáza I/II) preukázali ich dobrý bezpečnostný profil. V súčasnosti je v štádiu klinického testovania mnoho ďalších mikroenkapsulovaných bunkových systémov na liečbu hypotyreózy, atrofickej makulárnej degenerácie, Huntingtonovej choroby, Alzheimerovej choroby, alebo rakoviny pankreasu.
Nanomateriály ako nosiče liečiv
Využitie nanomateriálov v liečbe onkologických ochorení patrí k najintenzívnejšie sa rozvíjajúcim oblastiam medicíny, čo potvrdzuje aj množstvo spomínaných nanoproduktov schválených liekovými regulačnými agentúrami. Prísun živín do nádorovej masy je zabezpečovaný novovytvoreným cievnym systémom, ktorý svojou nedokonalou štruktúrou umožňuje intravenózne podaným nanoliečivám prednostnú akumuláciu práve v nádoroch (tzv. pasívne cielenie). Zvýšenie efektivity ich transportu do určeného tkaniva je možné docieliť úpravou povrchu nanonosiča naviazaním rôznych funkčných molekúl (ligandy, aptaméry, protilátky a pod.). Tieto molekuly sú špecifické pre nádorové bunky, čo umožňuje tzv. aktívne cielenie liečiva. Povrchové modifikácie zároveň zabraňujú rýchlej eliminácii nanoliečiva z krvného obehu a predlžujú dobu cirkulácie v krvi, čím zároveň zvyšujú pravdepodobnosť akumulácie liečiva v nádore. Nanonosiče pritom zabezpečujú aj stabilné a kontrolované uvoľňovanie liečiva zmenou pH, teploty, redoxným potenciálom (schopnosť látky viazať alebo uvoľňovať elektróny) a pod.
Fototermálna a fotodynamická terapia
Princípom týchto liečebných postupov je využitie tepla na zničenie nádorových buniek. Pri terapii sa využívajú nanomateriály, ktoré majú zvýšenú schopnosť absorbovať energiu svetla pri ožiarení, a uvoľňovať ju neskôr v podobe tepla. Po lokálnom podaní nanočastíc sa dané tkanivo vystaví hypertermii (prehriatie nad 42°C), vyvolanej ožiarením infračerveným svetlom. Nádorové bunky sú usmrtené tzv. termoabláciou, zatiaľ čo poškodenie okolitého zdravého tkaniva je minimálne. Pri fotodynamickej terapii sa terapeutický efekt zvyšuje pridaním okrem nanočastíc aj chemickej látky (fotosenzibilizátora), ktorá je taktiež schopná absorbovať energiu svetla. Pri uvoľnení energie z fotosenzibilátora dochádza k tvorbe toxických reaktívnych foriem kyslíka, čím sa znásobuje terapeutický efekt. Účinnosť fotodynamickej terapie závisí vo veľkej miere od účinnosti fotosenzibilizátorov a ich selektívneho dodávania do cieľového nádorového tkaniva. Liečbe onkologických ochorení pomocou fototermálnej a fotodynamickej terapie sa venuje značná pozornosť.
Imunoterapia
O nádoroch je známe, že sú schopné uniknúť pozornosti vlastného imunitného systému a zároveň ho využívať na podporu lokálneho rastu nádoru a metastáz. Cieľom imunoterapie zhubných nádorov je cielené dodávanie imunomodulačných buniek (dentritických buniek) a kostimulačných molekúl s využitím nanomateriálov. Takýto prístup predstavuje sľubnú liečebnú stratégiu v multimodálnej liečbe rôznych typov nádorov. Imunoterapia môže byť tiež použitá v kombinácii s inými liečebnými spôsobmi, ako je chemoterapia, fototerapia a génová terapia.
Imunoterapia sa využíva aj pri liečbe autoimunitných ochorení. Tieto chronické choroby vznikajú v dôsledku neprimeranej imunitnej reakcie proti vlastným antigénom, pričom majú za následok zápal a deštrukciu zdravých tkanív.
Perspektívy nanomedicíny
Využitie nanomateriálov a nanotechnológií v medicíne otvára nové inovatívne možnosti diagnostiky a liečby závažných civilizačných ochorení. Takou je napríklad personalizovaná terapia - perspektívna liečebná stratégia, ktorá zohľadňuje špecifiká pacienta a optimalizuje jeho terapiu (tzv. liečba šitá na mieru). Kľúčovou podmienkou pre klinické využitie nanomateriálov je ich biologická bezpečnosť. Pribúdajúce poznatky o interakciách nanočasticíc s bunkami, identifikácia parametrov nanočastíc, ktoré môžu vyvolávať nežiaduce účinky je základom pre vývoj nových, biologicky bezpečnejších nanočastíc pre klinické účely. Intenzívny výskum sa venuje novým spôsobom prípravy nanočastíc s využitím rastlín alebo mikroorganizov (tzv. zelená výroba), ktorý je ekologickejší v porovnaní s tradičnými postupmi prípravy.
Nanomedicína významnou mierou ovplyvní liečbu zhubných nádorov. Mnohé diagnózy, ktoré sa v súčasnosti nedajú vyliečiť, sa stanú v budúcnosti liečiteľné.







